镁纳米制剂调节软骨-成骨平衡,延缓骨关节炎进展
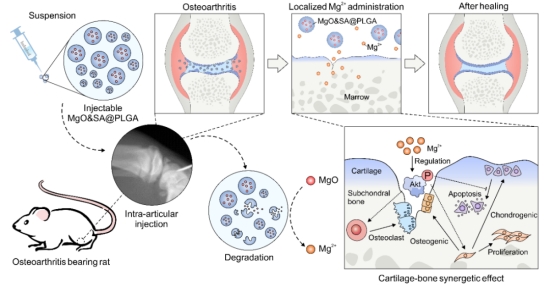
骨关节炎(Osteoarthritis,OA)作为最常见的骨关节退行性疾病,其保守治疗仍缺乏有效的手段。OA的病理进程主要表现为软骨、软骨下骨、滑膜等多种组织的退行性改变,因此,协同修复软骨及软骨下骨具有重要意义。一般来说,协同进行骨-软骨修复的策略有两种,一是利用药物载体协同递送多种药物进行修复,另一种则是寻找具有协同修复作用的药物及小分子。在本工作组前期的研究中发现,镁基金属降解产物镁离子具有较强的骨生物活性,且关节腔内补充镁离子可治疗OA,其作用机制尚未阐明,且缺乏有效的应用模式【1-3】。
近日,南京大学医学院附属鼓楼医院、南京大学现代应用与工程学院、浙江大学医学院附属第二医院、上海科技大学生命科学院、香港中文大学的蒋青、魏辉和张翼锋研究团队在Science Advances在线期刊发表了题为 Engineered MgO Nanoparticles for Cartilage-Bone Synergistic Therapy 的研究成果【4】。该研究发现镁离子能够通过调节软骨细胞、破骨细胞和成骨细胞中AKT的磷酸化水平,协同调控软骨与软骨下骨的病理进程,从而延缓骨关节炎的进展。基于这一机制,他们开发了一种工程化的用于OA的治疗的含镁制剂(MgO&SA@PLGA),并在动物实验中展开了转化研究。这项研究为开发基于镁的软骨-骨协同修复治疗策略提供了有力的科学依据,有望为改善OA患者的生活质量提供新的策略。

在伦理委员会的批准下,研究团队首先收集了南京鼓楼医院运动医学与成人重建外科进行全膝关节置换手术的软骨组织,在体外培养中发现,额外添加10 mM镁离子可以有效改善OA患者软骨的表型,同时抑制软骨的肥大化和矿化。这些结果表明,镁离子可以有效减少甚至逆转软骨组织的退行性改变。随后,研究人员对镁离子对多种与OA相关细胞的调控作用展开了研究,包括骨髓间充质干细胞(BMSCs)、软骨细胞和破骨细胞。他们发现,镁离子可以增强BMSCs的增殖和成软骨分化,并抑制其成骨分化,具有促进关节软骨再生的潜力。此外,镁离子还可以抑制软骨细胞的程序性死亡,从而保护关节软骨。对于破骨细胞,镁离子可以抑制其生成和骨降解功能。这些作用机制中,镁离子对不同细胞的磷酸化作用存在差异,这可能是由于不同细胞周围环境的差异导致的。
研究团队进一步对镁离子的关节腔内释放进行了优化。他们选择了氧化镁作为修饰核心,利用PLGA微球来稳定释放镁离子,并对氧化镁纳米颗粒进行表面改性以提高负载率和调节释放速率。他们在大鼠模型中进行了治疗实验,发现含镁微球可以改善OA大鼠的下肢稳定性和疼痛,并保护软骨和软骨下骨。这些结果表明,镁离子对软骨和软骨下骨的协同保护作用可能有望成为OA治疗的新策略。
总的来说,这项研究为镁离子在软骨-骨协同修复中的作用机制提供了新的认识,为OA的治疗提供了新的思路。未来的研究应该进一步探讨镁离子在不同细胞中的作用机制,进一步开展镁离子对骨/软骨重塑的调控机制研究,并优化镁离子的释放策略,以实现更好的治疗效果。
浙江大学医学院附属第二医院骨科郑力铭特聘研究员、南京大学现代工程与应用科学学院赵升博士、南京大学医学院附属鼓楼医院运动医学与成人重建外科李逸轩博士为本文的共同第一作者,南京大学医学院附属鼓楼医院骨科蒋青教授、南京大学现代工程与应用科学学院魏辉教授、上海科技大学生命科学学院张翼锋教授为本文共同通讯作者。
原文链接:https://www.science.org/doi/epdf/10.1126/sciadv.adk6084
|